Российские ученые классифицировали данные из крупнейшей базы онкогенных мутаций
На основании геномных данных 10 тыс. пациентов исследователи из лаборатории разработки инновационных лекарственных средств и агробиотехнологий Физтех-школы биологической и медицинской физики МФТИ подсчитали количество онкогенных мутаций молекулярных и функциональных типов в разных видах рака у пациентов различных демографических и клинических групп. Главной целью классификации было разделение мутаций на значимые и незначимые, чтобы в дальнейшем упростить подбор необходимой терапии, сообщили «МВ» в пресс-службе МВТИ. Результаты исследования опубликованы в журнале PLOS Genetics
«Смертность от рака составляет примерно половину случаев общей смертности, а мутации и различные хромосомные дефекты считаются главной причиной и одновременно механизмом развития рака. Мы анализируем их, чтобы выявлять мишени для потенциальных терапевтических воздействий, чтобы знать, на какие гены, на какие белки воздействовать», — пояснил один из авторов исследования, старший научный сотрудник лаборатории разработки инновационных лекарственных средств и агробиотехнологий МФТИ Алексей Беликов.
Для классификации мутаций, в том числе на значимые и незначимые, ученые разработали четыре биоинформатических алгоритма, с помощью которых обработали геномные данные из самой крупной базы данных пациентов с онкологией — TCGA PanCanAtlas.
Как уточнил Беликов, один из четырех алгоритмов выявляет онкогенные хромосомные дефекты, возникающие в опухолях. Причем делает это лучше, чем существующая до сих пор единственная в мире подобная американская программа, и выявленные дефекты подтверждаются другими научными исследованиями.
Среди большого количества мутаций и различных хромосомных аномалий новые алгоритмы позволили определять значимые для развития раковой опухоли. В частности, было выявлено, что в некоторых видах рака на развитие опухоли влияет только одна онкогенная мутация, а в некоторых — два десятка.
«Если взять образец опухоли конкретного пациента и отсеквенировать его, анализ может показать сотни мутаций, а для лечения придется подобрать ингибиторы сотни белков, что не представляется возможным, — отметил Беликов. — Наш анализ показывает, что в среднем значимыми оказываются 12 мутаций на опухоль, и это позволяет воздействовать именно на нужные белки, а не действовать вслепую».
Исследование позволило с высокой точностью определить количество различных типов онкогенных мутаций. Были проведены классификации по полу и возрасту пациентов, типу и стадии рака, а также по другим критериям.
Распределение онкогенных мутаций по типам рака
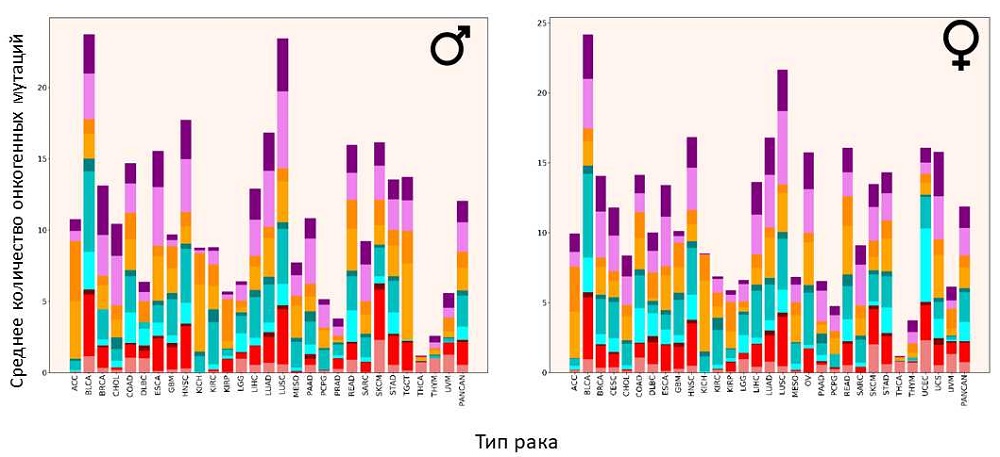 Источник: PLOS Genetics
Источник: PLOS Genetics
Распределение онкогенных мутаций по возрасту
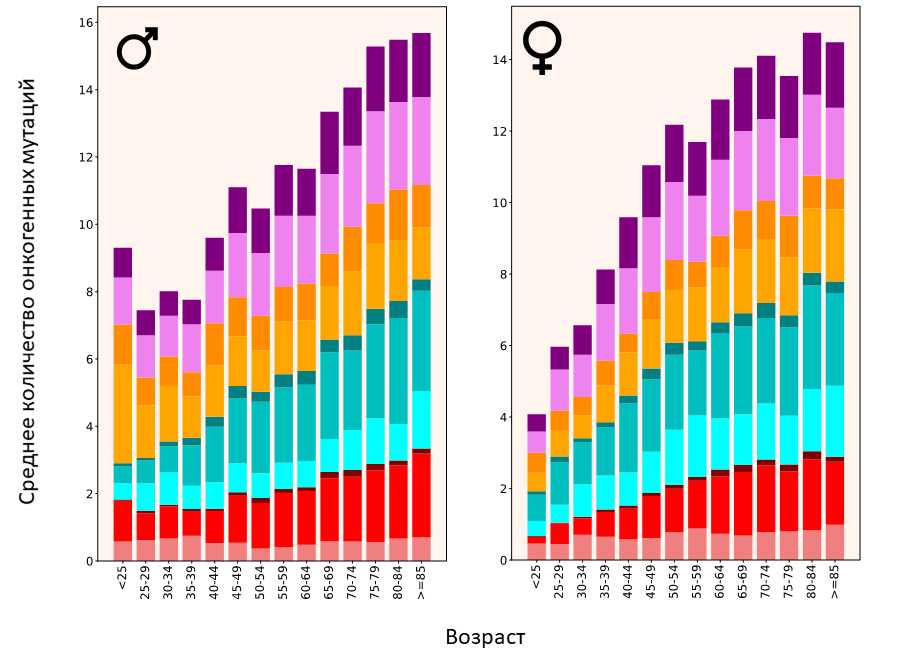
Источник: PLOS Genetics
Помимо ответов, проведенная классификация ставит большое количество вопросов и открывает перспективы для дальнейшей работы. Например, почему существует такая большая разница в количестве и составе онкогенных мутаций между типами рака? Почему для инициации рака щитовидной железы достаточно только одной онкогенной мутации, а при карциномах мочевого пузыря – несколько десятков? Почему у одних видов рака нет изменений в онкогенах, а у других нет изменений в опухолевых супрессорах? Объясняются ли эти различия разным тканевым микроокружением, к которому эти опухоли должны приспосабливаться? Почему тогда для некоторых пациентов с одним и тем же типом рака достаточно одной онкогенной мутации для развития обнаруживаемой опухоли, тогда как у других опухоли не диагностируются, пока не будут накоплены десятки мутаций?

Приведенная научная информация, содержащая описание активных веществ лекарственных препаратов, является обобщающей. Содержащаяся на сайте информация не должна быть использована для принятия самостоятельного решения о возможности применения представленных лекарственных препаратов и не может служить заменой очной консультации врача.
