Список по требованию: какие дефицитные медизделия входят в стандарты оснащения медучреждений
Непонятный ускоритель
Особенности обращения и государственной регистрации медизделий в случае их дефицита или риска его возникновения закреплены в Постановлении Правительства РФ № 552 от 01.04.2022. Согласно документу, перечень дефицитных медизделий должна утверждать межведомственная комиссия в Росздравнадзоре. Изделия из списка регистрируются по ускоренной процедуре.
Последняя редакция перечня была опубликована 11 августа. В нем 1667 наименований медизделий, включая реагенты, расходные материалы, оборудование для лабораторной диагностики и т.д.
Для участников рынка процедура включения продукции в список непрозрачная, заявил «МВ» вице-президент ассоциации «НП «ОПОРА», вице-президент Московской ассоциации малых предприятий — производителей медицинской техники «Асмедика», генеральный директор ООО «ГЕМ» Станислав Гольдберг.
«Пока не очень понятно, по какому принципу Росздравнадзор формирует этот перечень», — сказал он.
Руководитель одного из федеральных медицинских центров сообщил «МВ», что не следит за списком и «не понимает, на что он влияет».
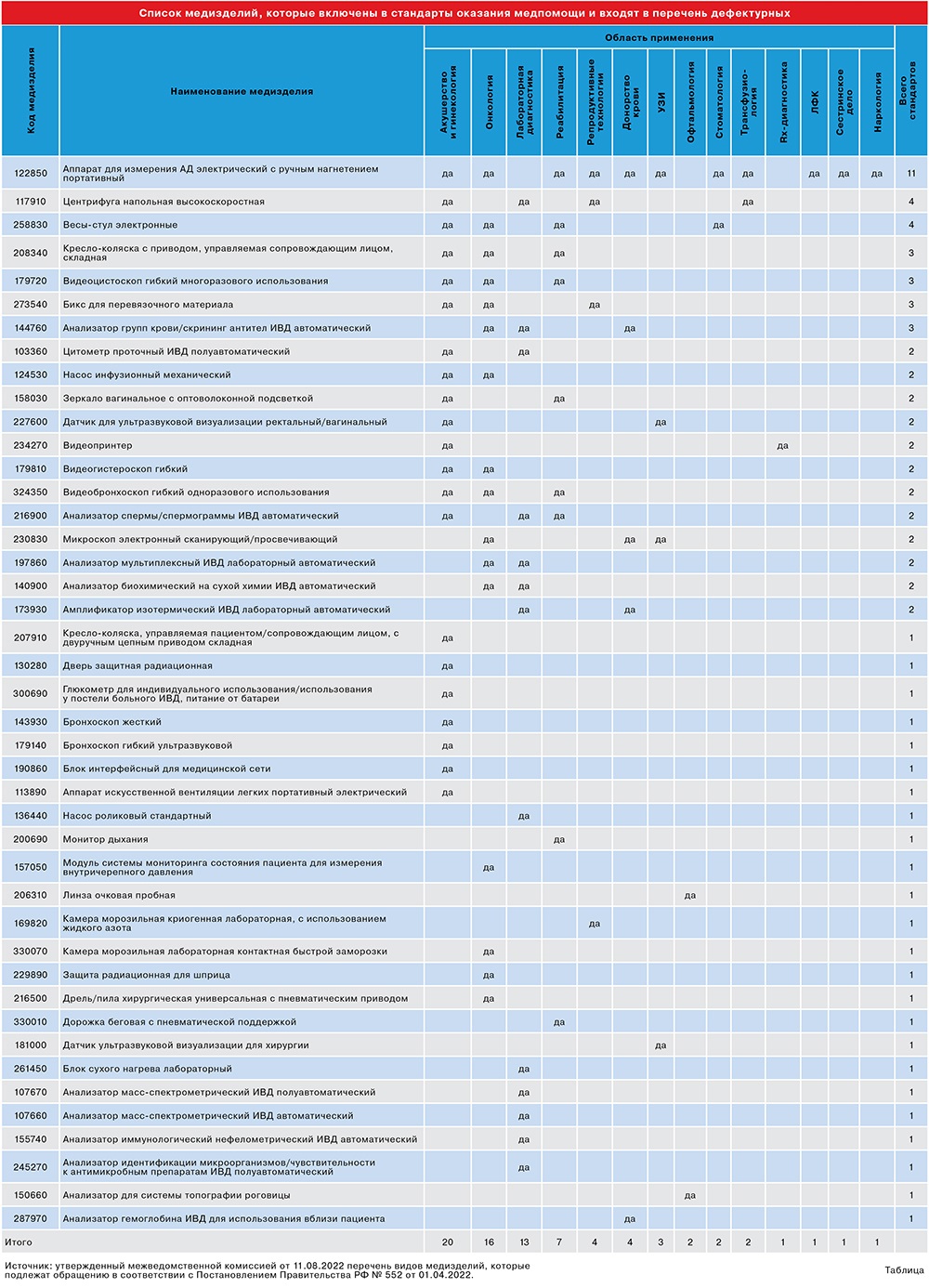
«МВ» проанализировал перечень и обнаружил минимум 43 изделия, которые входят в 14 стандартов оснащения отделений больниц, медицинских кабинетов и лабораторий (табл.). Большинство из них вошли в порядки оказания медпомощи по профилю «акушерство и гинекология» (приказ Минздрава РФ № 1130н от 20.10.2020), оказания помощи взрослому населению при онкологических заболеваниях (приказ Минздрава РФ № 116н от 19.02.2021), а также правил проведения лабораторных исследований (приказ Минздрава РФ № 4н от 18.05.2021).
Отсутствие на рынке необходимого оборудования может привести к несоблюдению медорганизациями стандартов оснащения, что оценивается проверяющими как нарушение лицензионных требований. Для госбольниц наказание за это предусмотрено ст.19.20 КоАП, для частных организаций — ст.14.1 КоАП. Размер штрафов может достигать 200 тыс. руб., в зависимости от степени вины и юридической формы собственности медучреждения.
Автономное плавание лабораторий
Представители лабораторий сообщили «МВ» об отсутствии проблем с оборудованием, в том числе включенным в «дефицитный» перечень.
Лаборатории «Инвитро» и Vet Union укомплектованы, и потребности в закупке нового оборудования нет, заверил «МВ» директор по закупкам и логистике «Инвитро» Сергей Пелевин. «При необходимости мы подбираем аналоги ушедшим с российского рынка производителям. Уже начали сотрудничать с турецкими и китайскими компаниями», — уточнил он.
Руководитель департамента развития продукта медицинской компании «ЛабКвест» Валерий Никитин отметил, что вошедшее в список дефектурных МИ лабораторное оборудование взаимозаменяемо и имеет альтернативы с немногочисленными изменениями в методиках выполнения исследований. «Не видим проблем в оснащении, доукомплектации нашей лаборатории или изменении парка оборудования. На рынке остаются некоторые европейские производители, предлагающие эти приборы», — сказал он «МВ».
Никитин добавил, что на российский рынок активно выходят китайские производители, но их приборы и реагенты регистрируются очень медленно, что не позволяет полностью закрыть текущие потребности лабораторий.
Регистрация на обычных условиях
С 1 января 2022 года Росздравнадзор прекратил прием заявок на регистрацию медизделий по национальным правилам в связи с переходом на регуляторику рынка Евразийского экономического союза (ЕАЭС). Однако еще в декабре прошлого года Совет Евразийской экономической комиссии (ЕЭК) одобрил изменения, согласно которым возможность национальной регистрации продлевалась до конца 2022 года. Изменения вступили в силу только после ратификации документа странами — участницами союза. В итоге регистрация медизделий в соответствии с российским законодательством возобновилась по факту только с 14 июня 2022 года.
В августе в рамках ЕАЭС были одобрены новые изменения, которые позволят регистрировать медизделия по национальным правилам вплоть до 2026 года. Проект протокола направили в страны союза для проведения внутригосударственных процедур. «МВ» направил запрос в ЕЭК с просьбой уточнить, какие государства уже ратифицировали документ.
Как сообщили «МВ» в пресс-службе Росздравнадзора, с января 2022 года в ведомство поступило больше 100 заявлений о регистрации медизделий в рамках ЕАЭС. На средину сентября выдано пока только одно регистрационное удостоверение (РУ).
С момента возобновления национальной регистрации медизделий Росздравнадзор получил 442 заявления на получение РУ по российскому законодательству. Выдано 66 удостоверений. По данным реестра Росздравнадзора, всего с 15 июня было выдано 1446 РУ на медизделия, включая те, которые заявлялись до 2022 года.

Приведенная научная информация, содержащая описание активных веществ лекарственных препаратов, является обобщающей. Содержащаяся на сайте информация не должна быть использована для принятия самостоятельного решения о возможности применения представленных лекарственных препаратов и не может служить заменой очной консультации врача.

